|
Capítulo 15: Sistema Excretor
Introducción Regresar
El medio interno, formado por los líquidos extracelulares que bañan a las células, recibe un continuo aporte de sustancias provenientes del aparato digestivo y del metabolismo celular. Pero las condiciones en el medio interno deben conservarse muy estables para mantener la vida y la salud.
El sistema excretor, por intermedio de su principal órgano, el riñón, está encargado de regular la cantidad de agua y la concentración de electrólitos y ciertos productos terminales del metabolismo en el líquido extracelular.
En el individuo sano, los riñones intercambian sustancias con el plasma para que el medio interno se mantenga constante. El sistema excretor o urinario realiza una continua filtración de la sangre, extrayendo del plasma una gran cantidad de sustancias que son eliminadas al exterior como orina.
La eliminación de sustancias desde el medio interno hacia el medio externo recibe el nombre de excreción.
La excreción urinaria permite eliminar, fundamentalmente:
• El exceso de agua
• El exceso de electrólitos
• Desechos nitrogenados del metabolismo
Entre las sustancias depuradas por orina también se encuentran los productos finales del metabolismo de la hemoglobina, metabolitos de hormonas y sustancias extrañas (agentes tóxicos, fármacos, plaguicidas, aditivos alimentarios).
La composición y volumen de la orina (diuresis) pueden variar ampliamente. Por ejemplo, si una persona bebe gran cantidad de agua, ésta tiende a diluir los líquidos corporales y aumentar su volumen, y el riñón responde con un aumento de la diuresis. En cambio, si una persona se ve privada de agua, los riñones producen una orina muy concentrada para disminuir al mínimo la pérdida de líquido. Del mismo modo, cuando hay déficit o exceso de potasio, ácido u otras sustancias, el riñón modifica su excreción para mantener en equilibrio el medio interno.
De esta forma, la composición y el volumen del medio interno sólo varían dentro de límites muy estrechos.
La insuficiencia renal altera la homeostasis del medio interno, conduciendo a una función anómala en todos los sistemas del cuerpo y en última instancia, a la muerte.
Desechos nitrogenados Regresar
Los desechos nitrogenados se originan del metabolismo celular y se vuelcan a la sangre, desde donde son incorporados a la orina cuando la sangre circula por el riñón. Si sus valores en sangre aumentan, ocasionan toxicidad.
Los desechos nitrogenados son:
• Urea: se genera a partir del grupo amino removido de los aminoácidos en el proceso de desaminación. La desaminación y la transformación del amino en urea (ciclo de la urea) tienen lugar principalmente en el hígado. La urea tiene la ventaja de ser un compuesto de bajo peso molecular, soluble en las membranas y por lo tanto fácilmente difusible. En la insuficiencia renal los valores de urea en sangre están anormalmente elevados, generando un síndrome conocido como uremia. Los síntomas de la uremia incluyen letargo, anorexia, náuseas, vómitos, deterioro mental y confusión, espasmos musculares, convulsiones y coma.
• Amoníaco: el amoníaco (NH3) o su catión amonio (NH4+) son los derivados inmediatos del grupo amino. Dada su alta toxicidad, el amoníaco es rápidamente convertido a urea. Cuando esta transformación no se produce, por ejemplo cuando hay una insuficiencia hepática, el amoníaco se acumula en sangre, provocando hiperamonionemia. Este síndrome incluye temblor, habla ininteligible, visión borrosa y, a concentraciones muy elevadas, daño cerebral irreversible, coma o muerte. La toxicidad del amoníaco afecta directamente al SNC.
• Ácido úrico: proviene del metabolismo de las bases púricas. Una producción incrementada o una excreción deficiente del ácido úrico causan la hiperuricemia. Como consecuencia, se depositan cristales de urato sódico en las articulaciones. Habitualmente se ve afectada una sola articulación, en el primer dedo del pie, provocando ataques de “gota” recidivantes. En los túbulos renales, el ácido úrico puede precipitar, dando lugar a la formación de cálculos.
• Creatina y creatinina: derivadas del metabolismo en la célula muscular.
Órganos del sistema excretor Regresar
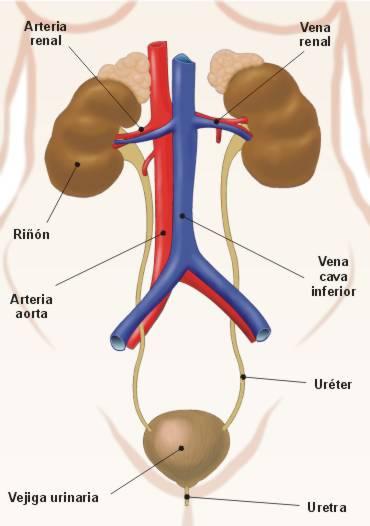 |
El aparato excretor está formado por los riñones, los uréteres, la vejiga urinaria y la uretra.
Los riñones son los órganos encargados de la formación de la orina. La orina es producida en el riñón en forma continua y volcada en los uréteres.
Los uréteres son dos largos conductos cilíndricos que conducen la orina desde los riñones, ubicados en la zona lumbar, hasta la vejiga urinaria, situada en la cavidad pélvica.
La vejiga urinaria es un órgano hueco, de pared músculo-membranosa, destinada a contener la orina. La vejiga actúa como un reservorio, donde la orina se acumula permanentemente, para ser expulsada en forma periódica. La capacidad fisiológica de la vejiga es de alrededor de 350 cc, con variantes individuales. Cuando se distiende más allá de esta capacidad, aparece el deseo de orinar. La expulsión de la orina recibe el nombre de micción.
La uretra es el órgano excretor terminal, por donde la orina se vuelca al exterior. El orificio externo de la uretra es el meato urinario.
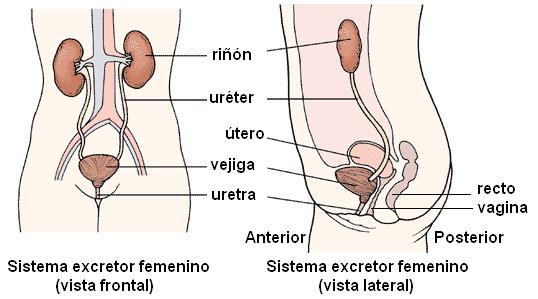
La uretra femenina es un órgano exclusivamente urinario. Mide unos 35 mm de longitud y, desde la vejiga, se dirige hacia abajo y adelante, adosada a la pared vaginal anterior. Desemboca en el meato urinario ubicado en el vestíbulo, entre los labios menores, por delante del introito vaginal.
 |
La uretra masculina es un órgano urogenital, pues además de recibir la orina y conducirla al exterior, también transporta el semen, que le llega a través de los conductos eyaculadores.
En el varón, la uretra mide unos 16 cm y posee tres porciones: prostática, membranosa y esponjosa. La porción prostática atraviesa la próstata de arriba de abajo y recibe las secreciones de esta glándula, las cuales contribuyen a la formación del semen. A la uretra prostática le sigue la porción membranosa, que atraviesa los músculos del periné, el piso de la pelvis. La última porción, la uretra esponjosa, es extrapélvica y transcurre por el interior del cuerpo esponjoso del pene. Desemboca en el meato urinario, ubicado en el glande.
Anatomía del riñón Regresar
El riñón es un órgano par, situado en la pared posterior de la cavidad abdominal, en la zona lumbar. Es un órgano retroperitoneal. Está cubierto por la cápsula renal, mide unos 12 cm de largo y pesa alrededor de 150 gramos.
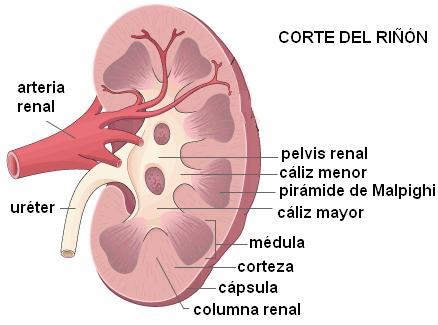
El riñón presenta un borde externo convexo y un borde interno cóncavo En este último se encuentra el hilio renal, a través del cual ingresan al riñón los vasos sanguíneos (la arteria renal y la vena renal), los nervios, y por donde emerge la pelvis renal. La pelvis renal es un ensanchamiento en forma de embudo, donde convergen los cálices renales, conductos que recogen la orina producida en el riñón. De la pelvis renal se origina el uréter.
Internamente, en el riñón se distinguen dos zonas: la externa, o corteza, y la interna, o médula.
La médula está recorrida por unas estructuras de disposición radial llamadas pirámides de Malpighi, de base externa y vértice interno, separadas por columnas. A la altura de los vértices, las pirámides de Malpighi presentan una zona cribosa (papila), por donde la orina drena hacia un cáliz, y de allí a la pelvis renal.
 |
Microscópicamente se puede reconocer a las unidades anatómicas y funcionales del riñón, los túbulos renales, también llamados nefronas o nefrones, las cuales se extienden tanto por la corteza como por la médula del órgano.
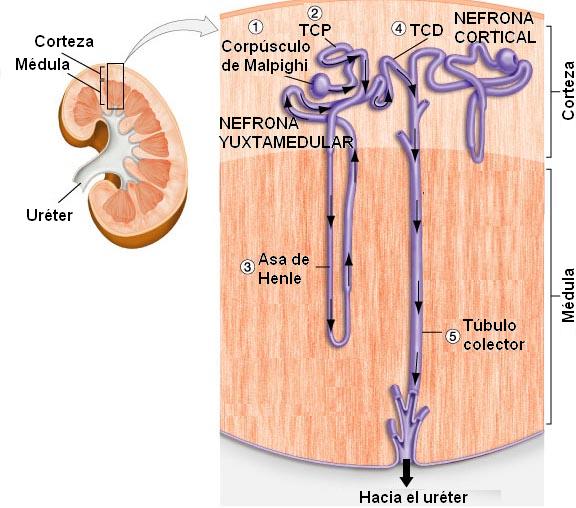 |
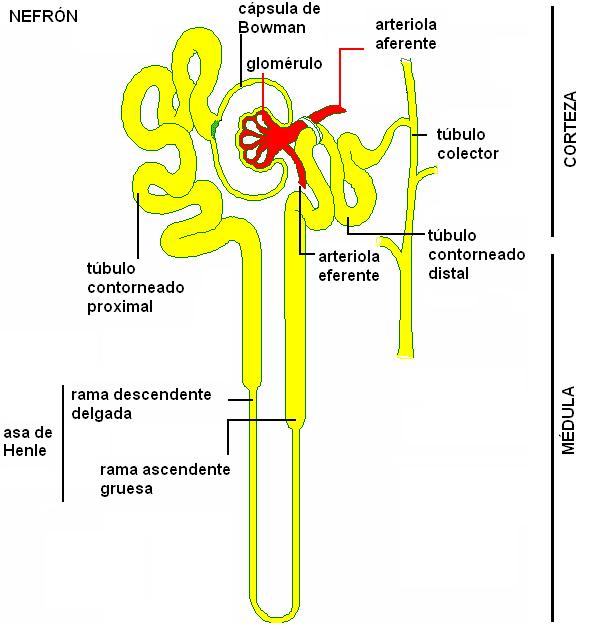
Las nefronas son túbulos que se inician con un extremo cerrado, mientras que su extremo opuesto se abre en un tubo colector. El extremo cerrado de la nefrona está hundido, formando una especie de copa, la cápsula de Bowman, en cuya concavidad se aloja un ovillo de vasos capilares que recibe el nombre de glomérulo. La asociación entre el glomérulo y la cápsula de Bowman se conoce como corpúsculo de Malpighi o corpúsculo renal.
A la cápsula de Bowman le sigue una porción flexuosa de la nefrona, el túbulo contorneado proximal (TCP). Tanto el corpúsculo de Malpighi como el túbulo contorneado proximal se ubican en la corteza renal.
El túbulo contorneado proximal se continúa con el asa de Henle (AH), un segmento que realiza un recorrido en forma de U, penetrando en la médula del riñón. El asa de Henle consta de una rama descendente, delgada, y una rama ascendente, gruesa.
Algunos nefrones, llamados corticales, poseen asas de Henle cortas; otros, los yuxtamedulares, cuyos corpúsculos de Malpighi se ubican muy cerca de la médula renal, presentan asas de Henle más largas. Estos últimos tienen importancia fisiológica, pues son los principales responsables de la concentración de la orina.
La última porción del nefrón se encuentra en la zona cortical; es un túbulo flexuoso, el túbulo contorneado distal (TCD), que desemboca en el conducto colector.
Varios túbulos contorneados distales provenientes de nefronas adyacentes desembocan en un tubo colector común. Éstos descienden desde la corteza hacia la médula y convergen en los cálices (en los vértices de las pirámides de Malpighi), los cuales se reúnen en la pelvis renal; de la pelvis renal nace el uréter.
La formación de la orina comienza en la cápsula de Bowman; la orina inicial es modificada mientras recorre el túbulo renal, hasta que es recogida en los cálices.
 |
Circulación renal Regresar
Los riñones filtran el plasma en forma continua. En un adulto, el 21% del gasto cardíaco pasa por el riñón, lo que implica que los riñones reciben alrededor de 1,2 litros de sangre por minuto.
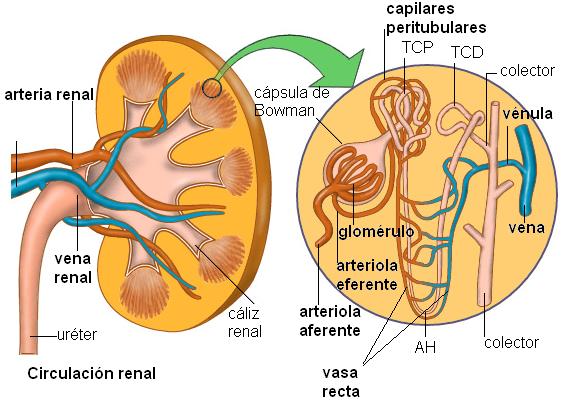
La sangre llega al riñón por una rama de la aorta, la arteria renal, que ingresa al órgano a través del hilio y se ramifica en su interior.
Cada nefrón recibe una rama arterial, llamada arteriola aferente, a partir de la cual se forma un ovillo capilar, el glomérulo, en íntimo contacto con la cápsula de Bowman. Allí tiene lugar la filtración. Luego, los capilares glomerulares confluyen formando una arteriola eferente, que se aleja de la cápsula.
La arteriola eferente se comporta de manera distinta, según el tipo de nefrón del cual provenga. Las arteriolas eferentes de los nefrones corticales se ramifican dando origen a una red de capilares peritubulares, que reciben esta denominación por su disposición alrededor de los túbulos que forman el nefrón.
Las arteriolas eferentes de los nefrones yuxtamedulares drenan no sólo en la red peritubular, sino que también se prolongan en los “vasa recta”. Los “vasa recta” forman asas que penetran en las pirámides medulares siguiendo a las asas de Henle.
Entre los capilares peritubulares, los “vasa recta” y la nefrona ocurre gran cantidad de intercambios.
Finalmente, los capilares peritubulares y los “vasa recta” forman vénulas que desembocan en la vena renal, la cual sale del órgano a nivel del hilio y drena en la vena cava inferior.
En el trayecto que realiza dentro del riñón, el plasma sufre modificaciones muy importantes relacionadas con la formación de la orina.
 |
Formación de orina Regresar
La orina se origina primariamente como un ultrafiltrado del plasma a nivel glomerular. Ya en el interior de los túbulos renales, este ultrafiltrado es modificado mediante dos procesos: reabsorción tubular y secreción tubular.
La reabsorción consiste en el transporte de sustancias, tanto agua como solutos, desde la luz tubular hacia los capilares sanguíneos peritubulares.
La secreción tubular es el transporte de sustancias desde los capilares peritubulares hacia los túbulos renales.
Significa que la orina definitiva ya no contiene gran parte de las sustancias filtradas, que son reabsorbidas, pero puede contener otras que no fueron filtradas, sino que se incorporaron a la luz tubular por un proceso de secreción posterior.
La excreción es entonces el resultado de la filtración glomerular, menos las sustancias reabsorbidas, más las sustancias secretadas.
FILTRACIÓN - REABSORCIÓN + SECRECIÓN = EXCRECIÓN |
Cada día unos 180 litros de sangre son filtrados en los riñones, de los cuales una pequeña parte es eliminada como orina.
Se denomina diuresis a la cantidad de orina excretada diariamente. La diuresis normal es de aproximadamente 1, 5 litros.
Filtración glomerular Regresar
La filtración glomerular consiste en el ultrafiltrado del plasma (plasma libre de proteínas) desde los capilares glomerulares hacia la luz tubular, más particularmente, hacia el espacio de la cápsula de Bowman.
El volumen y la composición del ultrafiltrado dependen de varios factores:
1. El flujo sanguíneo renal.
2. La barrera de filtración.
3. La diferencia de presión entre el glomérulo y la cápsula de Bowman.
1. El flujo sanguíneo renal es el volumen de sangre que circula por los riñones en la unidad de tiempo. La filtración glomerular es directamente proporcional al flujo sanguíneo renal. Por eso, el alto porcentaje del gasto cardíaco que llega al riñón se explica mejor como una forma de garantizar un flujo suficiente, que posibilite la filtración, que como una necesidad para abastecer a este órgano (aunque, de hecho, se trata de un órgano metabólicamente muy activo).
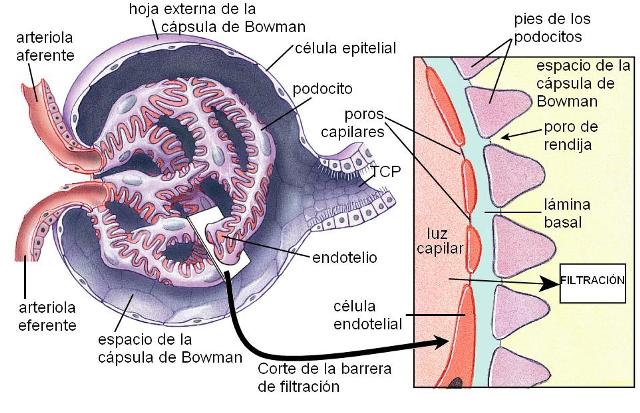
2. La barrera de filtración está constituida por el endotelio del capilar glomerular, la membrana basal y la hoja interna de la cápsula de Bowman.
Los capilares glomerulares son muy permeables, de tipo fenestrado, con un endotelio que presenta grandes poros.
La membrana basal está formada por una red de colágeno y proteoglicanos. Esta membrana deja pasar libremente al agua y los solutos pequeños, pero retiene a las proteínas. Los proteoglicanos de la membrana basal están cargados negativamente. Esto hace que, a igual diámetro de las partículas, las que están cargadas positivamente pasen con más facilidad que las negativas, que son repelidas por las cargas de la membrana basal.
La hoja interna de la cápsula de Bowman es una capa discontinua de células epiteliales, llamadas podocitos. Los podocitos tienen grandes expansiones parecidas a un pie, que rodean a los capilares glomerulares. Entre los pies hay espacios (los poros de rendija) por donde se desliza el filtrado glomerular.
La membrana glomerular es más gruesa que la de otros capilares, pero también es muy porosa, lo que la hace permeable. Los poros tienen un tamaño de 8 nm, aunque partículas más pequeñas, como la albúmina, no los atraviesan, debido a sus cargas negativas.
En conclusión, los únicos impedimentos para la filtración son el tamaño de las partículas y sus cargas.
La barrera de filtración retiene a las células sanguíneas y a las proteínas plasmáticas. El resto de los componentes del plasma pasa libremente hacia el espacio de la cápsula de Bowman.
 |
3. La filtración depende de la suma de presiones hidrostáticas y coloidosmóticas (oncóticas) que actúan sobre la barrera de filtración, favoreciendo la filtración u oponiéndose a ella.
Favorecen la filtración |
Se oponen a la filtración |
| Presión hidrostática glomerular (presión sanguínea) = 55 mm Hg |
Presión hidrostática en la cápsula de Bowman = 15 mm Hg |
Presión coloidosmótica en la cápsula de Bowman.
Esta fuerza es despreciable, ya que el filtrado prácticamente no contiene proteínas. |
Presión coloidosmótica glomerular = 30 mm Hg |
La presión efectiva de filtración resultante es:
Presión efectiva de filtración = 55 mm Hg – (15 mm Hg + 30 mm Hg) = 10 mm Hg
Reabsorción y Secreción en el nefrón: Túbulo Contorneado Proximal Regresar
La orina definitiva que llega a la pelvis renal se consigue tras la modificación del filtrado mediante los procesos de reabsorción y secreción tubular.
Casi el 99% del filtrado es reabsorbido en los túbulos renales. La reabsorción es un proceso selectivo. Mediante la reabsorción se recuperan para el organismo sustancias necesarias, como glucosa y aminoácidos, mientras que desechos, excesos de iones y otras sustancias, permanecen en el filtrado y son excretados con la orina.
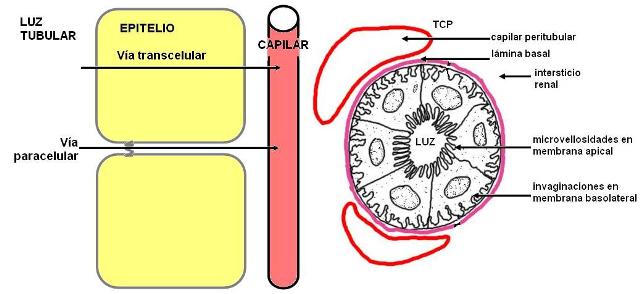
El transporte de sustancias entre el filtrado, en la luz de los túbulos renales, y el espacio intersticial, para acceder a los capilares sanguíneos, necesariamente debe realizarse a través del epitelio del túbulo renal.
Las sustancias transportadas pueden seguir la vía paracelular, a través de las uniones estrechas entre las células epiteliales, o la vía transcelular.
Las células del epitelio simple que forman el nefrón están adaptadas para la absorción. Poseen ribete en cepillo en su superficie apical e invaginaciones en la superficie basal; ambas diferenciaciones contribuyen a aumentar el área superficial de la membrana. Además contienen abundantes mitocondrias, necesarias para proveer la energía consumida en los transporte activos.
 |
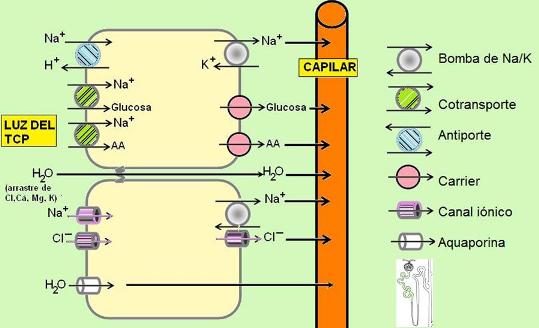
En el túbulo contorneado proximal se reabsorben el 70 % del agua, el sodio y el cloruro, la casi totalidad de la glucosa y los aminoácidos, vitaminas hidrosolubles y otros solutos filtrados.
La reabsorción de sodio en el TCP está determinada por la presencia de la bomba de Na+/K+ en la superficie basolateral del epitelio. La bomba extrae el sodio en la superficie basolateral, generando un gradiente que promueve el ingreso de este catión por la superficie apical. Como resultado, el sodio se mueve desde la luz tubular hacia la sangre.
El gradiente de sodio también es utilizado para la reabsorción de otras sustancias mediante un mecanismo de transporte activo secundario. En este tipo de transporte participa un cotransportador que moviliza simultáneamente dos solutos a través de la membrana. Uno de ellos es transportado a favor de gradiente, mientras que el otro se mueve contra gradiente. El cotransporte puede ser un simporte, si los dos solutos se trasladan en el mismo sentido, o un antiporte, cuando lo hacen en sentidos opuestos.
El simporte con sodio es el mecanismo que permite el ingreso de glucosa, aminoácidos y vitaminas por la superficie apical. Luego, estos solutos salen a favor de gradiente por la superficie basolateral, a través de sus carriers específicos.
Los carriers para glucosa ubicados en la superficie basolateral pertenecen a una familia de transportadores denominados GLUT. Cuando la concentración de glucosa plasmática (y por consiguiente en el filtrado) es alta, estos transportadores se saturan y no alcanzan a reabsorber toda la glucosa filtrada. A partir de entonces, la glucosa aparece en orina (glucosuria). Esto ocurre cuando la glucemia es mayor de 170 mg%, valor conocido como “umbral renal” para la glucosa.
De la misma forma, otras sustancias aparecen en orina cuando el filtrado contiene mayores concentraciones de las que pueden ser reabsorbidas, es decir cuando superan el umbral renal.
El antiporte con sodio también es responsable de la secreción de protones hacia la luz del TCP.
El gradiente de sodio favorable a su reabsorción acarrea cloruro, que es atraído por el gradiente eléctrico. El cloruro es transportado mediante canales iónicos, o bien por la vía paracelular.
El agua se reabsorbe por un gradiente osmótico, siguiendo a los solutos. Puede atravesar las células, por intermedio de canales específicos para el agua (aquaporinas), o el espacio paracelular. Cuando se mueve por la vía paracelular, ocasiona un “arrastre por solvente” llevando consigo solutos como calcio, cloruro, sodio, potasio y magnesio.
Las células del TCP también secretan aniones y cationes orgánicos, tanto endógenos (ácido úrico, oxalatos, adrenalina) como exógenos (penicilina, atropina, morfina).
Como el TCP es permeable tanto a los solutos como al agua, cuando el filtrado sale del TCP, es isotónico con el plasma.
 |
Asa de Henle Regresar
La rama descendente delgada del asa es impermeable a los solutos; sin embargo, es muy permeable al agua. Alrededor de un 15% del agua filtrada de reabsorbe en esta porción del nefrón.
La rama ascendente gruesa del asa de Henle es impermeable al agua, pero cuenta con mecanismos para el transporte activo de iones.
En la rama ascendente gruesa, la bomba de Na+/K+ en la superficie basolateral genera un gradiente de sodio, el cual permite la reabsorción del ión. Ésta se realiza acoplada con el transporte de cloruro y potasio, por intermedio de un cotransportador electroneutro. Dicho transportador introduce, simultáneamente, 1 sodio + 2 cloruros + 1 potasio. El cloruro es reabsorbido, pues abandona la superficie basolateral por difusión a través de un canal.
El potasio regresa a la luz a favor de gradiente. La acumulación de iones positivos en la luz genera una diferencia de potencial transepitelial. Esto impulsa la reabsorción de sodio, calcio y magnesio (cationes) por la vía paracelular.
Túbulo Contorneado Distal y Túbulo Colector Regresar
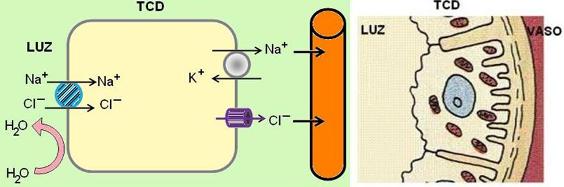
El TCD es impermeable al agua. La primera parte del TCD tiene propiedades semejantes al asa gruesa de Henle. Allí se realiza un transporte activo secundario de sodio con cloruro. Ambos son reabsorbidos. El primero, por la bomba Na+/K+, que genera el gradiente de sodio, y el segundo, mediante canales.
 |
La segunda parte del TCD tiene propiedades comunes con el túbulo colector. En estas porciones del nefrón distal hay dos clases de células: principales e intercalares.
Las células intercalares regulan el equilibrio ácido-base. Estas células pueden secretar protones (H+), cuando el medio interno se torna ácido, o bien bicarbonato (HCO3-), cuando el medio interno se torna alcalino.
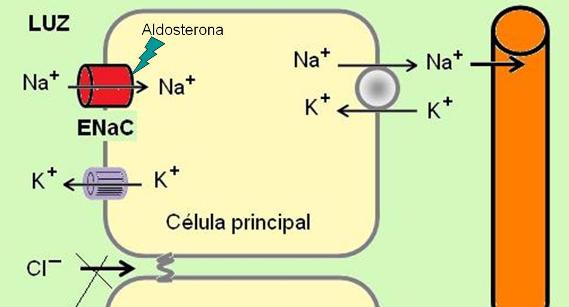
Las células principales reabsorben sodio y secretan potasio. El sodio ingresa por la superficie apical a través de unos canales especiales denominados “canales epiteliales de Na” (ENaC). La bomba de Na+/K+ en la superficie basolateral genera el gradiente de sodio y lo expulsa hacia el intersticio.
La reabsorción de sodio en el TC no se acompaña de reabsorción de cloruro, como ocurre en otros tramos del nefrón, debido que aquí el espacio paracelular es menos permeable. Esto hace que la luz se torne más negativa.
El potasio sale por los canales hacia la luz, siguiendo su gradiente de concentración y atraído por las cargas negativas de la luz tubular.
Los ENaC son sensibles a la hormona aldosterona. Un aumento de la aldosterona (un mineralocorticoide) incrementa la reabsorción de sodio y la secreción de potasio en el TC.
La absorción de agua en el túbulo colector es dependiente de la hormona antidiurética o vasopresina (HAD). En ausencia de HAD, el TC es impermeable al agua. La secreción de HAD estimula la reabsorción de agua en el TC.
 |
Resumen de los procesos de reabsorción y secreción en el nefrón Regresar
| Parte del nefrón |
Reabsorción de solutos |
Reabsorción de agua |
Secreción |
| TCP |
• 99% glucosa, aminoácidos, vitaminas hidrosolubles.
• 70% Na
• 80% K
• HCO3-
• Ca
• Mg |
SÍ |
• H+
• Aniones orgánicos
• Cationes orgánicos |
| Asa de Henle (Delgada) |
Impermeable |
Sí |
---------- |
| Asa de Henle (Gruesa) |
• Na
• Cl |
Impermeable |
---------- |
| TCD |
• Na (aldosterona)
• Cl (aldosterona) |
Impermeable |
• H+
• K (aldosterona) |
| TC |
• Na (aldosterona) |
No (s/HAD)
Sí (c/HAD)
|
• H+
• K (aldosterona) |
Mecanismo de concentración y dilución de la orina Regresar
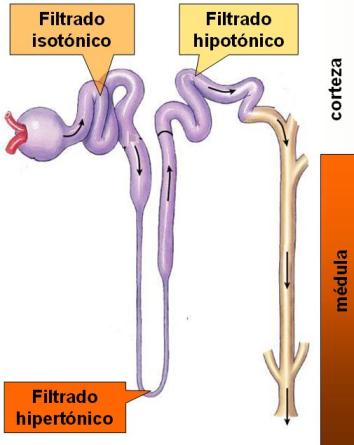
El filtrado que se produce en el glomérulo es isotónico con el plasma, ya que la filtración es un proceso no selectivo. La osmolaridad del plasma es de 300 mOsm/l.
En el TCP hay una importante reabsorción de solutos. Dado que el TCP es permeable al agua, ésta es reabsorbida por ósmosis, acompañando a los solutos. Por lo tanto, la osmolaridad del filtrado se mantiene.
Pero el líquido tubular se hace hipertónico cuando llega al asa de Henle descendente, ya que esta parte del nefrón es permeable al agua, pero no a los solutos. Así, el agua escapa hacia el espacio intersticial, en la médula renal, mientras que los solutos se concentran dentro del túbulo. En el extremo del asa, la osmolaridad del filtrado alcanza su máximo valor, de 1200 mOsm/l.
Este filtrado hipertónico asciende luego por el asa gruesa de Henle y el TCD. Ambos realizan reabsorción activa de iones, pero son impermeables al agua. La remoción de iones desde el líquido tubular hacia el intersticio, sin el acompañamiento de agua, vuelve a diluir el filtrado tubular. La osmolaridad del líquido tubular desciende paulatinamente, a medida que el filtrado asciende por el nefrón hacia la corteza. Cuando llega al TCD, el líquido es hipotónico.
 |
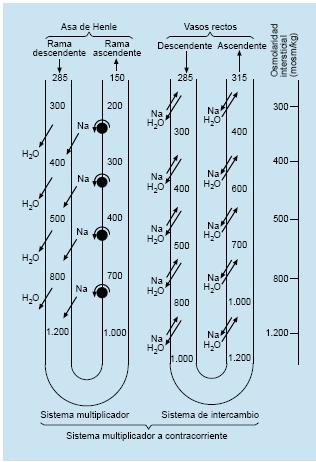
El Na+ bombeado fuera de la rama ascendente vuelve hipertónico el intersticio medular y, como la rama descendente del asa de Henle no permite la salida de Na+ pero sí su entrada desde el intersticio, la osmolaridad de éste aumenta de manera progresiva. El agua, por el contrario, fluye pasivamente desde la rama descendente del asa hacia el intersticio medular y, desde éste, hacia la rama ascendente. La proximidad anatómica entre ambas ramas permite por consiguiente un flujo de solutos a contracorriente desde la rama ascendente al intersticio y desde éste a la rama descendente, efecto que se multiplica a medida que se profundiza en la región medular (mecanismo multiplicador de contracorriente). Como resultado, la osmolaridad aumenta tanto en el interior del túbulo renal como en el intersticio medular, creándose un fuerte gradiente osmótico entre la región cortical y la medular.
El intercambio a contracorriente es el proceso que permite conservar la hipertonicidad intersticial creada por el asa de Henle y se basa en la particular disposición anatómica de los vasos rectos medulares. Si éstos se limitaran a atravesar linealmente la región medular, perderían agua y ganarían solutos a partir del intersticio renal hipertónico por simple difusión, lo cual ocasionaría una disminución continuada de la hipertonicidad intersticial. Por el contrario, los vasos rectos descendentes (arteriolas) se continúan con los vasos rectos ascendentes (vénulas), de trayecto paralelo y sentido contrario. En su recorrido descendente, los vasos pierden agua y ganan solutos, mientras que en su trayecto ascendente, el agua fluye hacia su interior y los solutos hacia fuera.
La sangre que circula por el interior de los vasos rectos medulares se equilibra en todo momento con la osmolaridad intersticial. Esta disposición en paralelo de los vasos rectos medulares, y el consiguiente intercambio de solutos a contracorriente, evita que la circulación renal disipe el esfuerzo del asa de Henle en crear una fuerte hipertonicidad medular.
 |
Además del cloruro de sodio, la urea contribuye en importante medida a generar la hipertonicidad del intersticio medular. Parte de la urea filtrada que llega al túbulo colector es reabsorbida desde este último hacia el asa de Henle y los vasos rectos. De esta forma la urea recircula continuamente por la médula renal, aumentando la concentración de solutos del intersticio.
¿Cuál es la importancia fisiológica de crear un intersticio cada vez más hipertónico, a medida que se desciende desde la corteza hacia la médula? Regresar
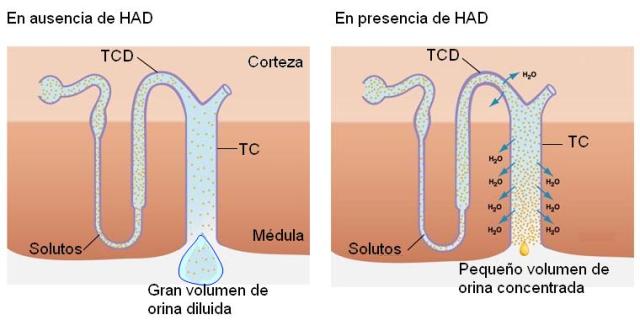
Obsérvese que la última porción del nefrón, el túbulo colector, realiza este recorrido. El TC recibe una orina hipoosmótica. En ausencia de HAD, el TC es impermeable al agua. Por lo tanto, excretará una orina hipoosmótica, es decir diluida, con baja concentración de solutos y gran volumen de agua.
Sin embargo, si el organismo necesita retener agua, deberá excretar la menor cantidad posible de ésta, concentrando la orina.
Cuando falta agua en el organismo, se estimula la secreción de HAD. La HAD hace al TC permeable al agua. Así, a medida que la orina desciende por el TC, desde la corteza hacia la médula, se encuentra con un medio cada vez más hipertónico, que ejerce atracción sobre el agua. El agua abandona el TC, mediante un proceso osmótico, hasta lograr una orina concentrada. La máxima concentración que puede lograrse en el riñón humano es la que se consigue en el intersticio medular, de 1200 mOsm/l.
La osmolaridad del plasma es captada por osmorreceptores ubicados en el hipotálamo. Cuando la osmolaridad plasmática aumenta, los osmorreceptores detectan el cambio y el hipotálamo pone en marcha los mecanismos homeostáticos:
- La sed, que alerta sobre la necesidad de incorporar agua.
- La secreción de HAD, que es liberada desde la neurohipófisis. De esta forma, se reabsorbe agua en TC, disminuyendo la osmolaridad plasmática.
 |
El mecanismo de acción de la HAD en el TC consiste en aumentar el número de aquaporinas de la membrana apical. Este efecto se consigue estimulando la migración y la fusión con la membrana plasmática de vesículas citoplasmáticas que reservan aquaporinas en estado no funcional.
Composición final de la orina Regresar
La orina excretada es un líquido límpido, de color amarillo ámbar, con escasos sedimentos. Su volumen, osmolaridad, densidad y pH son sumamente variables, ya que dependen de los mecanismos compensatorios del riñón para mantener la homeostasis.
La orina contiene agua; cloruro de sodio; sulfatos; fosfatos de sodio, de calcio y magnesio y pequeñas cantidades de amoníaco.
Entre las sustancias orgánicas, las principales son la urea, el ácido úrico, la creatina, la creatinina, los pigmentos biliares, enzimas y metabolitos de hormonas.
El análisis de orina tiene un importante valor diagnóstico. Son índice de alteraciones la glucosuria, la albuminuria y la presencia de células sanguíneas, entre otros.
Micción Regresar
La micción es un acto reflejo espinal, controlado por centros cerebrales superiores, que como la defecación está sujeto a inhibición o facilitación voluntarias.
Durante la micción se contrae la vejiga y se relajan el esfínter uretral externo y los músculos perineales.
Otras funciones del riñón Regresar
Además de las ya mencionadas, el riñón desempeña otras funciones:
• Secreción de eritropoyetina. La eritropoyetina es una hormona glucoproteica que actúa sobre células madres de la médula ósea, estimulando su diferenciación hacia la producción de eritrocitos.
• Secreción de renina. La renina es un hormona secretada por el aparato yuxtaglomerular del riñón.
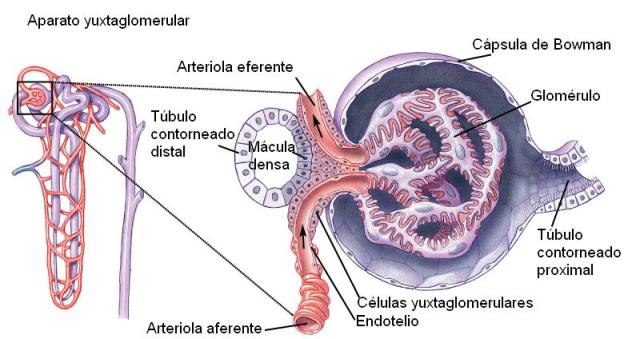
El aparato yuxtaglomerular está formado por las células yuxtaglomerulares, la mácula densa y las células extraglomerulares.
Las células yuxtaglomerulares están localizadas en la arteriola aferente, en su entrada al glomérulo. Son células epitelioides, que contienen los gránulos secretores de renina.
La mácula densa es una región modificada del túbulo contorneado distal, que se pone en contacto con la arteriola aferente.
Las células extraglomerulares son células agranulosas localizadas en la unión entre las arteriolas aferente y eferente. También secretan renina.
 |
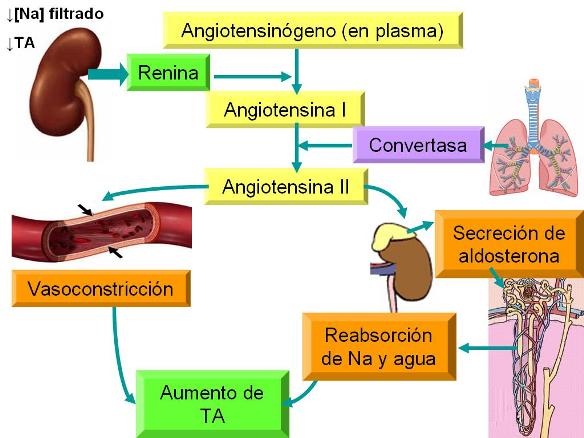
La función de la renina consiste en activar el angiotensinógeno plasmático, al convertirlo en angiotensina I. La angiotensina I, a su vez, es convertida a angiotensina II por la enzima convertasa, presente en el endotelio de los vasos del pulmón y otros órganos.
La angiotensina II es uno de los vasoconstrictores más potentes. Produce constricción arteriolar y aumenta la presión arterial sistólica y diastólica.
Además, estimula la secreción de aldosterona en la corteza suprarrenal, con el consecuente aumento de la reabsorción de sodio en el túbulo renal. Como el sodio arrastra agua por ósmosis, se produce un aumento de la volemia, contribuyendo aún más al incremento de la presión arterial.
 |
La secreción de renina es regulada por diferentes factores. Uno de ellos es la presión que trae la sangre cuando llega a la arteriola aferente. La arteriola aferente posee barorreceptores (receptores de presión) que detectan la presión sanguínea intraarteriolar, estimulando la secreción de renina cuando la presión arterial disminuye e inhibiéndola cuando la presión arterial es alta.
La secreción de renina también es estimulada ante una disminución de la cantidad de sodio que llega a la mácula densa.
|
|
