|
Capítulo 14: Sistema Respiratorio
Introducción Regresar
Las células de nuestro organismo, como la mayoría de los seres vivos (exceptuando a ciertas bacterias) necesitan un aporte continuo de oxígeno (O2) para llevar a cabo la respiración celular. Como resultado de este proceso, las células generan dióxido de carbono (CO2), gas que debe ser eliminado. El sistema respiratorio es el conjunto de órganos que nos permiten intercambiar oxígeno y dióxido de carbono con el medio circundante.
Una serie de procesos se relacionan con la función respiratoria; en ellos no sólo interviene el aparato respiratorio, sino que también participan el aparato circulatorio y todos los tejidos, donde se efectúa la respiración celular. Dichos procesos son:
• Ventilación: flujo de aire entre el exterior y los pulmones.
• Hematosis o respiración externa: difusión de oxígeno y dióxido de carbono entre los alvéolos pulmonares y la sangre.
• Transporte de gases en sangre: traslado de oxígeno desde los pulmones hasta las células y de dióxido de carbono desde las células hasta los pulmones.
• Respiración interna o tisular: difusión de oxígeno y de dióxido de carbono entre la sangre y los tejidos.
• Respiración celular.
El sistema respiratorio comprende los siguientes órganos: fosas nasales, faringe, laringe, tráquea, bronquios y pulmones. Los cuatro primeros forman la vía respiratoria, cuya función es la conducción del aire. Los pulmones son los órganos donde se cumple el intercambio gaseoso.
En primer lugar describiremos los órganos respiratorios y luego analizaremos cada uno de los procesos mencionados.
Fosas nasales Regresar
Las fosas nasales son dos largos túneles delimitados por los huesos de la cara y del cráneo, cuya abertura anterior está cubierta por la nariz. Un tabique intermedio separa a la fosa izquierda de la derecha.
Por delante, las fosas nasales se comunican con el exterior a través de los orificios nasales o narinas. Por detrás, cada fosa se comunica con la faringe a través de un orificio llamado coana.
Las paredes laterales de las fosas nasales presentan tres eminencias, los cornetes superior, medio e inferior, entre los cuales se encuentran espacios denominados meatos.
El interior de las fosas nasales está revestido por una membrana mucosa, la pituitaria. En ésta se distinguen dos zonas: la superior u olfatoria de coloración amarillenta, donde se ubican los receptores del olfato y la inferior o respiratoria, más rosada, pues posee una abundante irrigación. La membrana pituitaria presenta células ciliadas y células productoras de moco. A la altura de los orificios nasales la pituitaria se continúa con la piel, donde se desarrollan folículos pilosos.
Cuando pasa por las fosas nasales, el aire es modificado de tres formas: 1) el aire se calienta, por el contacto con la extensa superficie que ofrecen los cornetes y el tabique; 2) el aire se humidifica casi por completo; y 3) el aire se filtra. En la filtración colaboran los pelos que se hallan a la entrada, los cuales retienen las partículas más grandes que están suspendidas en el aire. Pero más importante es la turbulencia que generan los cornetes; cuando el aire choca contra los cornetes, cambia de dirección y las partículas quedan adheridas a la capa de moco. Luego las cilias barren el moco con las impurezas hacia la faringe; desde allí es deglutido.
Estas funciones de las fosas nasales determinan el acondicionamiento del aire y son muy importantes para proteger a los pulmones del enfriamiento y la desecación.
Faringe Regresar
La faringe es un órgano común a los aparatos digestivo y respiratorio. Comunica a la boca con el esófago, por un lado, y a las fosas nasales con la laringe, por el otro. Funciona como una vía de paso para el bolo alimenticio y el aire.
La laringe se ubica en la parte anterior del cuello. Es un conducto formado por siete cartílagos: dos pares (aritenoides y corniculados) y tres impares (epiglotis, tiroides y cricoides), unidos por ligamentos y músculos.
El cartílago tiroides presenta un ángulo saliente que se puede palpar a través de la piel y se conoce como “nuez de Adán”.
La epiglotis funciona como una tapa que desciende y cubre la entrada a la laringe durante la deglución, para desviar el bolo alimenticio hacia el esófago.
En el interior de la laringe se encuentran dos pares de cuerdas vocales: las superiores, también llamadas falsas, y las inferiores o verdaderas. El espacio comprendido entre las cuerdas vocales se denomina glotis. Cuando el aire sale a través de la glotis, el grado de tensión o relajación de las cuerdas vocales produce distintas vibraciones. Estos movimientos generan los sonidos. Por lo tanto, la laringe no solo forma parte de la vía respiratoria, sino que es además el principal órgano de la fonación.
Tráquea Regresar
La tráquea es un tubo flexible, aplanado en la parte posterior, de aproximadamente 12 cm de longitud y 2 cm de ancho, que recorre parte del cuello y del tórax.
Sus paredes presentan una serie de anillos cartilaginosos que le dan sostén e impiden su colapso. Estos anillos no son círculos completos, pues presentan una interrupción en su cara posterior, que se halla cerrada por músculo.
La tráquea se bifurca en un ángulo denominado “carina”, dando origen a los bronquios fuente.
La función de la tráquea es la conducción del aire desde la laringe hacia los bronquios.
Bronquios Regresar
Son dos cilindros huecos que resultan de la bifurcación de la tráquea. El bronquio derecho es algo más vertical y más corto que el izquierdo. Cada bronquio penetra en el pulmón correspondiente, dentro del cual se ramifica formando ramas cada vez menores. Las últimas ramas del árbol respiratorio, los bronquíolos, son los encargados de conducir el aire a los alvéolos pulmonares.
Pulmones Regresar
Los pulmones son los órganos esenciales del aparato respiratorio. Se ubican en la cavidad torácica, separados por un espacio llamado mediastino. Cada pulmón tiene la forma de un semicono, con su cara plana orientada hacia el mediastino y su superficie convexa en contacto con la pared torácica. La base de los pulmones apoya sobre el músculo diafragma y el vértice llega a la altura de la primera costilla.
La coloración es rosada en el niño, grisácea en el adulto y gris oscuro en el anciano.
Los pulmones tienen una consistencia blanda y son muy elásticos; ceden a la presión fácilmente y rápidamente recobran su forma.
En la superficie de los pulmones se observan hendiduras profundas, llamadas cisuras, que separan los lóbulos pulmonares; el pulmón derecho comprende tres lóbulos y el izquierdo, dos.
La cara interna de los pulmones presenta una zona denominada hilio, por donde ingresan al pulmón los bronquios, los vasos sanguíneos y los nervios.
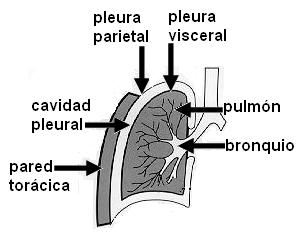 |
Las pleuras son las membranas serosas que recubren los pulmones. Cada pleura está formada por una hoja parietal, en contacto con la pared torácica, y una hoja visceral, adherida a la superficie del pulmón. La hoja visceral se continúa con la parietal a la altura del hilio. Entre ambas hojas hay un espacio virtual, la cavidad pleural, ocupada por una delgada película líquida. Las pleuras facilitan el deslizamiento de los pulmones dentro de la cavidad torácica.
En ciertas situaciones patológicas, la cavidad pleural deja de ser virtual y se llena de aire (neumotórax), o sangre (hemotórax). Al aumentar la presión dentro de la cavidad (que habitualmente tiene presión negativa), los pulmones son comprimidos, con la consecuente dificultad respiratoria.
Internamente, los pulmones están recorridos por el árbol bronquial, cuyas ramificaciones más delgadas, los bronquíolos respiratorios, terminan en los sacos alveolares. Cada saco alveolar tiene el aspecto de un racimo de uvas, y está formado por varios alvéolos.
Los alvéolos son las unidades anatómicas y funcionales del pulmón. Son pequeños sacos, de 0,1 mm de diámetro. Presentan paredes muy delgadas, formadas por una sola capa de células epiteliales aplanadas, y se hallan rodeados por una gran red capilar. Entre ambos pulmones poseen unos 300 millones de alvéolos, cuya área superficial equivale a 70 metros cuadrados. La delgadez de la membrana alveolar, la cercanía a los capilares y su amplia superficie son las características que facilitan el intercambio gaseoso que ocurre en los alvéolos.
En el epitelio alveolar, además de las células ya mencionadas, se encuentran otras, menos numerosas, especializadas en la secreción de un surfactante. El surfactante es un fosfolípido que cubre toda la superficie del alvéolo y contribuye a mantenerlo distendido, ya que actúa disminuyendo la tensión superficial. También son frecuentes los macrófagos, encargados de la eliminación de agentes extraños.
Ventilación Regresar
La ventilación es la renovación del aire pulmonar. La ventilación se logra por medio de una mecánica respiratoria, un conjunto de movimientos que producen la entrada del aire a los pulmones – la inspiración- y la salida del aire de los mismos – la espiración- a través de la vía respiratoria.
El principal músculo respiratorio es el diafragma. La inspiración es causada por la contracción del diafragma.
Cuando el diafragma se contrae, se hace más plano y se desplaza hacia abajo. El descenso del diafragma aumenta el diámetro longitudinal del tórax. Normalmente, entre la pared torácica y los pulmones existe tan solo una delgada capa de líquido. Los pulmones se resisten a ser separados de la pared, de la misma manera que dos piezas de vidrio mojadas resisten la separación. Por lo tanto, cuando se distiende la pared torácica, los pulmones lo hacen junto a ésta. Este fenómeno se denomina “solidaridad tóraco-pulmonar”.
Cuando aumenta el volumen del tórax y solidariamente el volumen pulmonar, la presión intrapulmonar desciende, haciéndose menor que la presión atmosférica. Ya que el aire se mueve desde la zona de mayor a la de menor presión, esta diferencia de presión hace que el aire ingrese a la vía respiratoria, causando el movimiento de inspiración.
La espiración normal es un fenómeno pasivo, que ocurre cuando el diafragma se relaja. La relajación del diafragma provoca su ascenso, con la consecuente disminución de los volúmenes torácico y pulmonar. Así, la presión dentro del tórax aumenta, hasta que supera a la presión exterior. Como resultado, el aire abandona los pulmones y es expulsado al exterior.
En la respiración tranquila normal, el trabajo del diafragma alargando y acortando la cavidad torácica es suficiente para producir la inspiración y la espiración.
En la respiración enérgica, sin embargo, se requiere la participación de otros músculos respiratorios accesorios que elevan y bajan las costillas, aumentando o disminuyendo el diámetro anteroposterior del tórax.
Los músculos más importantes que elevan las costillas son los intercostales externos. También contribuyen accesoriamente los escalenos, elevando las dos primeras costillas, el serrato anterior, levantando las costillas, y el esternocleidomastoideo, que eleva el esternón. Estos últimos cobran mayor importancia en situaciones de dificultad respiratoria.
Los músculos que hacen descender las costillas durante la espiración son los intercostales internos. Los músculos rectos del abdomen tiran las costillas hacia abajo y junto a otros músculos abdominales, comprimen el contenido abdominal hacia arriba, contra el diafragma, colaborando en la espiración forzada.
Los pulmones realizan 12 movimientos inspiratorios y espiratorios en el término de un minuto. Esta cifra es la frecuencia respiratoria normal o eupnea. Se denomina taquipnea al aumento de la frecuencia respiratoria y bradipnea a la disminución de la misma.
Volúmenes y capacidades pulmonares Regresar
El volumen de aire que se moviliza en la ventilación es variable y depende de los movimientos realizados y de la elasticidad pulmonar.
La suma de distintos volúmenes permite obtener las capacidades pulmonares.
• Volumen corriente: es el volumen de aire que se inspira y espira en una respiración normal; es de 500 ml.
• Volumen de reserva inspiratoria: es el volumen de aire que ingresa al pulmón en una inspiración forzada que sigue a una inspiración normal; corresponde a 3.000 ml.
• Volumen de reserva espiratoria: es el volumen que se puede expulsar en una espiración forzada, después de una espiración normal. Son unos 1.100 ml.
• Volumen residual: hay unos 1200 ml que siempre permanecen en los pulmones y no pueden eliminarse ni aun en espiración forzada. A ese volumen se lo llama volumen residual.
• Capacidad vital: es la mayor cantidad de aire que puede ser espirada después de un esfuerzo espiratorio máximo. Es la suma del volumen corriente y los volúmenes de reserva inspiratoria y espiratoria. Equivale a 4.600 ml.
• Capacidad pulmonar total: todos los volúmenes suman una capacidad pulmonar total de 5.800 ml.
Los volúmenes pulmonares son aproximadamente un 20% menores en la mujer que en el varón.
Si se multiplica la frecuencia por el volumen corriente, se obtiene la cantidad de aire que los pulmones renuevan en 1 minuto, la que equivale a 6 litros.
Hematosis (respiración externa) Regresar
La hematosis es el intercambio de oxígeno y de dióxido de carbono que se realiza entre el aire que llega a los alvéolos y la sangre que circula por los capilares alveolares. Este intercambio se produce a través de la membrana respiratoria, formada por las delgadas paredes de los alvéolos (un epitelio plano simple), el endotelio capilar y sus respectivas membranas basales, que pueden estar fusionadas.
La hematosis consiste en un movimiento neto de oxígeno desde el aire alveolar hacia la sangre, y de dióxido de carbono desde la sangre hacia el aire alveolar. Dichos movimientos corresponden a un fenómeno de difusión.
La difusión de los gases a través de la membrana respiratoria depende de los siguientes factores:
1. Presión parcial del gas. Las moléculas de los gases que forman el aire se hallan en constante movimiento. El impacto causado por las moléculas sobre la superficie de la vía respiratoria y de los alvéolos es la presión del gas. La presión del aire depende de la concentración total de partículas de gas.
La presión total del aire a nivel del mar es de 760 mm Hg o torr (=1 atmósfera). Sin embargo, como el aire es una mezcla de gases, cada gas contribuye a la presión total en proporción directa a su concentración. La presión que ejerce cada gas en particular es la presión parcial de ese gas. Por ejemplo, la presión parcial del oxígeno en el aire corresponde a unos 160 mm Hg, es decir al 20,84% de la presión total, ya que éste es el porcentaje de oxígeno en el aire.Los gases disueltos en los líquidos corporales también ejercen sus propias presiones parciales al encontrarse con una superficie, como la membrana celular.
| Composición del aire atmosférico |
| Gas |
Porcentaje del total |
| Nitrógeno (N2) |
78,62% |
| Oxígeno (O2) |
20,84% |
| Dióxido de carbono (CO2) |
0,04% |
| Vapor de agua |
0,50% |
La difusión de los gases es directamente proporcional a su diferencia de presión parcial. El gradiente de presión parcial de cada gas entre el aire alveolar y la sangre es el factor determinante de la difusión.
La sangre llega a los capilares pulmonares a través de la arteria pulmonar. Ésta transporta sangre carboxigenada proveniente de los tejidos (es la única arteria que transporta sangre “venosa”). La presión parcial de CO2 en el extremo arterial de los capilares es de 46 mm Hg, mayor que la del aire alveolar, de 40 mm Hg. El gradiente de presión parcial impulsa la salida del CO2 hacia el alvéolo. Cuando la sangre sale de la red capilar, en el extremo venoso, la presión parcial de CO2 es de 40 mm de Hg.
Por su parte, el O2 llega a los capilares alveolares con una presión de 40 mm Hg. Como su presión parcial en el aire alveolar es de 100 mm Hg, este gas difunde hacia la sangre. Así, al llegar al extremo venoso de la red capilar alveolar, la presión parcial de O2 alcanza unos 95 mm de Hg: la sangre se ha oxigenado.
Las venas pulmonares, que transportan la sangre oxigenada hacia el corazón izquierdo, son las únicas venas con sangre “arterial”.
El aire alveolar no tiene las mismas concentraciones de gases que el aire atmosférico. Existen varias razones para estas diferencias. 1) El aire alveolar sólo es sustituido parcialmente en cada ventilación. 2) Se está absorbiendo oxígeno continuamente del aire alveolar. 3) El dióxido de carbono difunde constantemente desde la sangre. 4) El aire alveolar, a diferencia del atmosférico, está saturado de vapor de agua, ya que se humidifica a su paso por la vía respiratoria.
Con respecto al N2, su presión parcial prácticamente no varía. Esto es debido a la ausencia de un gradiente, ya que el N2 no es consumido ni generado en las células.
2. Solubilidad del gas. Depende de la afinidad entre el gas y el solvente. Los gases de importancia respiratoria son muy solubles en las membranas, pues son afines a los lípidos. La mayor limitación que encuentra el movimiento de los gases en los tejidos no se debe a su solubilidad en las membranas, sino a su solubilidad en el agua de los líquidos corporales. El CO2 es alrededor de 20 veces más soluble que el O2.
3. Peso molecular. La difusión es inversamente proporcional al peso molecular del gas.
4. Espesor de la membrana. Cuanto mayor sea el espesor de la membrana, mayor será la distancia a recorrer, y más lenta la difusión. La membrana respiratoria es muy delgada. Sin embargo, en algunas patologías (como fibrosis o edema pulmonar), este espacio puede estar engrosado, dificultando la hematosis.
5. Área de la superficie de intercambio. La difusión es directamente proporcional al área de intercambio. El área superficial de la membrana respiratoria es muy extensa, como ya se mencionara al describir la estructura del pulmón. Transporte de gases en sangre e intercambio con los tejidos Regresar
| Transporte de O2 en sangre |
| En disolución en el plasma |
3% |
| Como oxihemoglobina |
97% |
Una vez que el oxígeno ha difundido desde los alvéolos a la sangre, es transportado a los capilares tisulares, donde se libera para ser utilizado por las células.
El oxígeno es transportado en la sangre de dos formas: disuelto en el plasma y unido a la hemoglobina.
La solubilidad del oxígeno en el plasma es muy baja, por lo que esta forma de transporte resulta insuficiente para hacer frente a la demanda de los tejidos. Tan sólo un 3% del total de oxígeno presente en la sangre es transportado en disolución.
El 97% del oxígeno que ingresa a la sangre es captado rápidamente por la hemoglobina (Hb)en el interior de los glóbulos rojos. La presencia de la hemoglobina permite a la sangre transportar entre 30 y 100 veces más oxígeno del que podría ser transportado simplemente disuelto en el agua de la sangre.
La molécula de Hb posee 4 grupos hemo; en cada uno de ellos hay un átomo de hierro capaz de unirse con una molécula de O2, formando la oxihemoglobina.
Para actuar como un transportador eficaz, la hemoglobina no solo debe poder unirse al oxígeno, también debe poder cederlo allí donde sea necesario.
La unión entre el oxígeno y la hemoglobina es una unión reversible; así, el oxígeno se combina con la hemoglobina en los capilares pulmonares y se disocia de ésta en los capilares sistémicos. De esta forma la oxihemoglobina transporta el oxígeno desde el pulmón hasta los tejidos.
La formación y la disociación de la oxihemoglobina dependen de la presión parcial de oxígeno. A altas presiones parciales, como las del pulmón, un alto porcentaje de la hemoglobina está combinado con oxígeno. En cambio, a bajas presiones, como las de los tejidos, el porcentaje de hemoglobina que está ligada con oxígeno es mucho menor.
Se denomina porcentaje de saturación de la hemoglobina al porcentaje de la misma que se encuentra combinada con oxígeno, como oxihemoglobina.
El siguiente gráfico representa el porcentaje de hemoglobina ligada con oxígeno a diferentes presiones parciales del gas. Es la curva de saturación de la hemoglobina, leída de izquierda a derecha, o bien de disociación de la oxihemoglobina, si lee de derecha a izquierda. Es una curva de tipo sigmoidea.
El gráfico permite observar que en los extremos de la curva, tanto a altas como a bajas presiones de oxígeno, los cambios de presión no se traducen en grandes cambios en los porcentajes de saturación.
Por ejemplo, a una presión de oxígeno de 100 mm Hg, como la de los pulmones, el 97 % de la hemoglobina se encuentra saturada. La curva es casi horizontal entre los 100 mm Hg y los 60 mm Hg de presión parcial; a este último valor, el porcentaje de saturación aún es del 90%. Significa que los cambios en la presión parcial de oxígeno a nivel pulmonar influyen poco en la saturación.
En el otro extremo de la curva, a presiones menores de 10 mm Hg, los cambios de presión también tienen poca influencia en la saturación.
Pero a valores de presión parcial comprendidos entre 60 y 10 mm Hg, la curva se hace casi vertical. El descenso abrupto de la curva en este tramo indica que pequeñas disminuciones de la presión parcial de oxígeno provocan una acelerada disociación de la oxihemoglobina. Esto significa que cuando la sangre arterial pasa por los tejidos, cuya presión parcial de oxígeno está comprendida en ese rango, gran parte de la oxihemoglobina se disocia, permitiendo la difusión de oxígeno hacia las células.
A una presión parcial de 40 mm Hg, cual es la de un tejido en actividad normal, el porcentaje de saturación es del 75%, o sea que un 25% de la oxihemoglobina está disociada. A una presión de 20 mm Hg, como la de un tejido en intensa actividad, con alto consumo de oxígeno, el porcentaje de saturación es del 25%, vale decir que el 75% de la hemoglobina ha cedido el oxigeno que llevaba unido.
En otras palabras: la hemoglobina tiende a captar el oxígeno en donde éste abunda (en los pulmones) y a liberarlo en donde éste escasea (en los tejidos).
La forma sigmoidea de la curva de disociación de la hemoglobina se explica por la interacción entre las subunidades de globina que forman la molécula. La hemoglobina existe en dos conformaciones: tensa y relajada. La forma tensa es poco afín al oxígeno, mientras que la forma relajada tiene mayor afinidad. Cuando una molécula de oxígeno se une a un grupo hemo, la estructura de la globina cambia de la forma tensa a la relajada. Ese cambio se transmite a las otras subunidades, que se hacen más afines al oxígeno. De esta forma, el ingreso de oxígeno a una subunidad facilita la entrada del oxígeno a las siguientes.
Inversamente, la disociación de una molécula de oxígeno de una subunidad la devuelve a su forma tensa. Este cambio de conformación influye en las demás subunidades, que también adquieren la forma tensa, disminuyendo su afinidad por el oxígeno. Así, la liberación de oxígeno de una subunidad favorece la liberación en las subunidades restantes.
La interacción entre las subunidades de globina, llamada efecto cooperativo, es la causante de la parte abrupta de la curva de disociación.
El efecto cooperativo entre las subunidades de globina y su consecuencia, la variación de la afinidad de la hemoglobina por el oxígeno en función de las presiones parciales de éste, hacen de la hemoglobina un excelente transportador.
La respiración tisular o interna es el intercambio de gases entre la sangre y las células. Dado que los tejidos consumen el O2 en la respiración celular, poseen siempre una baja presión parcial de este gas. En conclusión, cuando la sangre arterial pasa a través de los tejidos por los capilares sistémicos, la oxihemoglobina se disocia y el oxígeno difunde hacia las células. Al salir la sangre por el sistema venoso, la presión de oxígeno en la misma es de 40 mm Hg.
El dióxido de carbono es un producto de la respiración celular. Las células generan dióxido de carbono continuamente y por eso su presión parcial es más alta en los tejidos que en la sangre. Entonces el dióxido de carbono difunde desde los tejidos hacia los capilares sistémicos, siguiendo su gradiente de presión.
A consecuencia de estos intercambios, la sangre proveniente del sistema arterial de la aorta, que ingresa a la red capilar de los tejidos como sangre oxigenada, sale de ella convertida en sangre carboxigenada. Ésta se dirige de retorno al corazón derecho por intermedio de las venas cavas, completando así el circuito mayor.
| Transporte de CO2 en sangre |
| En disolución en el plasma |
7% |
| Como bicarbonato (HCO3) |
70% |
| Unido a hemoglobina |
23% |
Hay tres formas de transporte para el dióxido de carbono. Una parte del dióxido de carbono que ingresa a la sangre se disuelve en el plasma y así es transportada hasta los alvéolos. Esta fracción equivale al 7% del total.
Sin embargo, la mayor parte del dióxido de carbono difunde hacia los glóbulos rojos. En el interior de los glóbulos, la enzima anhidrasa carbónica cataliza la combinación del dióxido de carbono con el agua, obteniéndose el ácido carbónico (H2CO3). Este último se disocia, liberando un protón y el anión bicarbonato (HCO3-). Los protones son captados por la hemoglobina cuando ésta cede el oxígeno. El bicarbonato difunde hacia el plasma en los capilares sistémicos. La salida del bicarbonato tiene lugar mediante un transportador que lo intercambia por el anión cloruro, manteniendo la neutralidad eléctrica.
El bicarbonato en el plasma es la forma de transporte más importante para el dióxido de carbono, pues equivale a un 70 % del total del gas transportado.
El 23 % restante se combina con la hemoglobina. El dióxido de carbono se une a los extremos aminoterminales de las cadenas de globina, formando unos compuestos denominados carbamatos.
Cuando la sangre carboxigenada llega al pulmón, la hemoglobina en los glóbulos rojos se satura de oxígeno. La unión del oxígeno desplaza protones de la molécula de hemoglobina. El bicarbonato ingresa a los glóbulos rojos (por antiporte con cloruro) y se combina con los protones formando nuevamente ácido carbónico. Este último se descompone, (reacción catalizada por la anhidrasa carbónica) produciendo dióxido de carbono y agua. La formación de oxihemoglobina en los pulmones también favorece la separación del dióxido de carbono unido a la hemoglobina en forma de carbamatos El dióxido de carbono difunde entonces hacia el alvéolo, siguiendo su gradiente de presión.
Factores que influyen en la afinidad entre hemoglobina y oxígeno Regresar
La cantidad de oxígeno que se combina con la hemoglobina es influida por varios factores, además de la presión parcial de oxígeno, como ya se mencionó. Dichos factores son:
1. Presión parcial de CO2: cuando la presión parcial de CO2 aumenta, la oxihemoglobina tiende a disociarse del oxígeno. Esto contribuye a la función normal, porque en los capilares periféricos la presión de CO2 es elevada, lo que ayuda a la sangre a desprenderse del oxígeno. La disminución de la afinidad entre la hemoglobina y el oxígeno causada por el CO2 se conoce como “efecto Bohr”.
2. pH: el aumento de la acidez tiende a expulsar oxígeno de la molécula de hemoglobina. Esto también tiene utilidad fisiológica, ya que en los tejidos el pH es menor que en la sangre arterial. Cuanto más activo es un tejido, menor es su pH. El descenso del pH está relacionado con dos factores. Uno es la formación de CO2, que genera ácido carbónico, el cual se ioniza liberando un protón. El otro factor es el ácido láctico. Este compuesto se forma en el tejido muscular cuando la actividad es muy intensa. El ácido láctico también contribuye a aumentar la concentración de protones.
3. Temperatura: elevadas temperaturas disminuyen la afinidad entre oxígeno y hemoglobina. Dicho efecto tiene lugar en los músculos, donde la temperatura aumenta con el ejercicio. Igual que los factores anteriores, éste contribuye a aumentar la disponibilidad de oxígeno en el tejido muscular en actividad.
4. 2,3-DPG (2,3-difosfoglicerato): este compuesto se fija a la molécula de hemoglobina entre sus subunidades, haciéndola menos afín al oxígeno. El 2,3-DPG es un compuesto normal del glóbulo rojo, pero se encuentra aumentado en situaciones de hipoxia (baja disponibilidad de oxígeno). Por ejemplo, el 2,3-DPG aumenta en los fumadores o a grandes altitudes, favoreciendo la liberación de oxígeno hacia los tejidos. La hemoglobina fetal, a diferencia de la hemoglobina del adulto, no se une al 2,3-DPG. Esta diferencia es de suma importancia durante el embarazo, ya que causa la cesión del oxígeno desde la hemoglobina materna (menos afín al oxígeno) hacia la fetal (más afín al oxígeno).
Todos los factores mencionados, al disminuir la afinidad entre la hemoglobina y el oxígeno, causan un desplazamiento de la curva de saturación de la hemoglobina hacia la derecha. Significa que, en presencia de los mismos, se requieren mayores presiones parciales de oxígeno para alcanzar el mismo porcentaje de saturación que en su ausencia.
Derivados de la Hemoglobina Regresar
El hierro presente en el grupo hemo debe hallarse como ión ferroso (Fe2+) para poder ligar la molécula de oxígeno. La metahemoglobina se forma cuando el ión ferroso se oxida a ión férrico (Fe3+). Esta conversión inhabilita a la hemoglobina para el transporte de oxígeno.
La metahemoglobinemia (metahemoglobina en sangre) puede deberse a defectos genéticos o a la acción de ciertos fármacos.
No debe confundirse la hemoglobina oxidada (metahemoglobina) con la hemoglobina oxigenada, que es la hemoglobina normal combinada con oxigeno (oxihemoglobina).
La carboxihemoglobina es la combinación de la hemoglobina con el monóxido de carbono (CO). Este gas se forma como producto de la combustión incompleta de compuestos orgánicos.
El CO compite con el O2 por su unión a la hemoglobina, pero su afinidad por aquélla es 210 veces mayor que la del O2. Esta propiedad lo convierte en un compuesto sumamente tóxico, ya que la hemoglobina combinada con CO no puede transportar oxígeno. La intoxicación con CO es una causa frecuente de muerte en la estación invernal, cuando se calefaccionan las viviendas con estufas que producen combustión incompleta.
La hemoglobina glicosilada se forma lentamente por combinación entre la hemoglobina y la glucosa-6-fosfato. En los individuos diabéticos, cuya glucemia tiene valores por encima de los normales, el porcentaje de hemoglobina glicosilada es más alto. La determinación de la hemoglobina glicosilada en un análisis de sangre puede utilizarse como índice de la glucemia en los 2 ó 3 meses previos a la toma de la muestra (no tiene valor más allá de ese período, ya que los glóbulos rojos se renuevan cada 120 días).
Respiración celular: Conceptos generales Regresar
La respiración celular es el proceso de conversión de la energía química de las moléculas combustibles en energía utilizable en las células vivas. La respiración celular es una forma de combustión en la cual los enlaces químicos de las moléculas orgánicas se rompen y la energía del enlace queda disponible para realizar un trabajo celular.
El combustible celular por excelencia es la glucosa. La combustión de la glucosa se inicia en el citosol, en una etapa que recibe el nombre de glucólisis (ruptura de la glucosa). Las etapas finales de la respiración celular tienen lugar en un organoide citoplasmático, la mitocondria. Otros combustibles diferentes de la glucosa, (los ácidos grasos y los aminoácidos) también pueden ingresar a la respiración celular en la etapa mitocondrial.
Durante la respiración celular las moléculas combustibles son transformadas y ocurren tres procesos simultáneos e interrelacionados:
1) Descomposición: los combustibles son degradados hasta dióxido de carbono. Los procesos que transforman las sustancias complejas (como los combustibles) en sustancias más simples (como el dióxido de carbono) se denominan procesos catabólicos.
Como la energía química de las moléculas se encuentra almacenada en sus enlaces, todo proceso catabólico, en el cual se rompen enlaces químicos, va acompañado de una liberación de energía. Los fenómenos en los cuales la energía es liberada reciben el nombre de procesos exergónicos.
2) Oxidación: la oxidación consiste en una pérdida de hidrógeno (H+ y e-) o bien en una ganancia de oxígeno. La oxidación de los combustibles tiene lugar mediante un proceso de deshidrogenación. Los átomos de hidrógeno separados del combustible son transferidos temporariamente a coenzimas transportadoras de hidrógeno, las cuales los ceden a un aceptor final. El proceso contrario a la oxidación se denomina reducción. Las moléculas que actúan como aceptoras de protones y electrones se reducen.
En la respiración celular, el oxígeno es el aceptor final que resulta reducido al recibir los protones y electrones transportados por las coenzimas. Esta es la razón por la cual las células necesitan un suministro constante de oxígeno, proveniente del exterior.
El oxígeno se combina con el hidrógeno transferido desde las coenzimas, formando agua. Esto último ocurre en la etapa mitocondrial.
Los procesos de oxidación son exergónicos. Por lo tanto, durante la transferencia de hidrógeno desde los combustibles hasta el oxígeno, se libera una gran cantidad de energía.
3) Transferencia de energía: en los procesos exergónicos, inevitablemente una parte de la energía se convierte en calor. La energía calórica no es útil, pues no puede ser empleada para propulsar trabajos celulares. Dicha energía se disipa en el ambiente. Así se pierde aproximadamente el 60% de la energía que se libera en los procesos de descomposición y oxidación del combustible.
Pero el 40% restante de la energía se utiliza para la síntesis de ATP. La energía almacenada en el ATP es energía fácilmente utilizable por las células. El ATP puede ser considerado el principal producto de la respiración celular.
En conclusión, la respiración celular es un proceso catabólico, oxidativo y exergónico. Los sustratos de la respiración celular son los combustibles y el oxígeno, más ADP y P, en tanto que sus productos finales son dióxido de carbono, agua, ATP y calor.
| Metabolismo |
| Transformaciones de la Materia |
Anabolismo |
Transformación de sustancias simples en sustancias complejas (síntesis). |
| Catabolismo |
Transformación de sustancias complejas en sustancias más simples (degradación). |
| Procesos Redox |
Liberación de H+ y e-. |
| Ganancia de H+ y e-. |
| Transformaciones de la Energía |
Procesos Exergónicos |
Liberan energía. Ejemplos: reacciones catabólicas, procesos de oxidación. |
| Procesos Endergónicos |
Requieren energía. Ejemplos: reaccciones anabólicas, reacciones de reducción, trabajos celulares (transporte activo, contracción, etc.) |
Coenzimas Regresar
Una coenzima es una molécula orgánica no proteica que establece una unión débil y transitoria con una proteína catalítica (apoenzima). La unión de la apoenzima con la coenzima conforma una enzima conjugada funcional, también llamada holoenzima.
Muchos de los procesos metabólicos son reacciones de óxido-reducción o redox, en las cuales simultáneamente un compuesto se oxida y otro se reduce.
Las reacciones redox son catalizadas por enzimas conjugadas que contienen una coenzima transportadora de hidrógeno. Las coenzimas transportadoras de hidrógeno actúan como intermediarias, transfiriendo los H+ y e- desde la reacción de oxidación a la de reducción.
Dichas coenzimas existen en dos estados interconvertibles:
- El estado oxidado: en el que están disponibles para captar los H+ y e- liberados por el compuesto que se oxida.
- El estado reducido: en el que portan H+ y e-, los cuales ceden al compuesto que será reducido. |
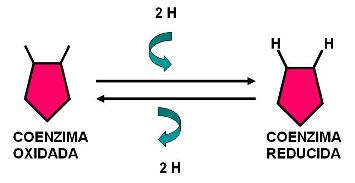 |
Las coenzimas transportadoras de hidrógeno que participan en la respiración celular son los dinucleótidos NAD+ y FAD.
El NAD+ (nicotinamín-adenín dinucleótido) puede transportar un par de electrones y un H+, que se incorporan a su estructura, más un H+ en unión iónica.
El FAD (flavín-adenín dinucleótido) transporta dos átomos de H (2 H+ y 2 e-).
La coenzima A (CoA) es intermediaria en reacciones de transferencia de grupos acilo (radicales de ácidos carboxílicos) y como tal cumple un papel importante durante la respiración celular.
El NAD+, el FAD y la coenzima A son derivados de distintos compuestos que forman parte del complejo vitamínico B.
Procesos aeróbicos y anaeróbicos Regresar
Algunas células, como los glóbulos rojos, carecen de mitocondrias, por lo que solamente realizan la primera etapa, llamada glucólisis, que no requiere la presencia de oxígeno. Los procesos que se llevan a cabo sin intervención del oxígeno reciben el nombre de anaeróbicos, en contraposición a aquellos que requieren oxígeno, llamados aeróbicos. La cantidad de energía acumulada en ATP que se obtiene de la oxidación anaeróbica es menor que la obtenida en la respiración aeróbica, ya que durante la misma la oxidación del combustible es incompleta.
Las células musculares poseen mitocondrias, pero tienen la facultad de realizar oxidación anaeróbica cuando el suministro de oxígeno resulta insuficiente, por ejemplo durante un ejercicio intenso.
Glucólisis: etapa común de los procesos aeróbicos y anaeróbicos Regresar
La glucólisis (“ruptura de la glucosa”) es la primera etapa de la oxidación, tanto aeróbica como anaeróbica. Durante la glucólisis no se requiere la presencia de oxígeno. Esta etapa se lleva a cabo en el citosol.
La glucólisis consta de 9 pasos, al cabo de los cuales la molécula de glucosa resulta parcialmente catabolizada. Cada paso es catalizado por una enzima diferente.
Paso 1. La molécula de glucosa es fosforilada. Una molécula de ATP se hidroliza y su grupo fosfato es transferido al C 6 de la glucosa. Se obtienen glucosa 6-fosfato y ADP.
Paso 2. La glucosa 6-fosfato es convertida a su isómero, la fructosa 6-fosfato.
Paso 3. La fructosa 6-P es fosforilada en el C 1. El grupo fosfato es donado por una molécula de ATP. Se obtienen fructosa 1,6-difosfato y ADP.
Paso 4. La molécula de fructosa 1,6-difosfato es escindida en dos triosas: 3-fosfogliceraldehído y dihidroxiacetona fosfato. Esta última se isomeriza rápidamente a 3-fosfogliceraldehído. Ambas moléculas de 3-fosfogliceraldehído siguen la misma ruta de transformaciones. Por lo tanto, de aquí en adelante, al realizar el balance, todas las reacciones deben contarse 2 veces.
Paso 5. El 3-fosfogliceraldehído se fosforila en el C 1, adicionando un grupo fosfato inorgánico. Simultáneamente el 3-fosfogliceraldehído se deshidrogena con la concomitante reducción del NAD+. El producto de ambas transformaciones es el 1,3-difosfoglicerato (forma ionizada del ácido fosfoglicérico). La unión del grupo fosfato en posición 1 se convierte en una unión de alta energía.
Paso 6. El grupo fosfato de alta energía es transferido desde el 1,3 difosfoglicerato al ADP. Los productos de la reacción son ATP y 3-fosfoglicerato. La fosforilación directa del ADP se denomina “fosforilación a nivel de sustrato”. Esta es la primera reacción de la glucólisis en la que se cosecha ATP.
Paso 7. El 3-fosfoglicerato se isomeriza a 2-fosfoglicerato.
Paso 8. El 2-fosfoglicerato pierde una molécula de agua. El grupo fosfato del C 2 se convierte en un grupo fosfato de alta energía. La molécula obtenida se denomina fosfoenolpiruvato.
Paso 9. Es la segunda fosforilación a nivel de sustrato. De la misma resultan ATP y piruvato.
En conclusión, durante la glucólisis una molécula de glucosa es dividida en dos triosas, que luego se oxidan, convirtiéndose en dos moléculas de ácido, el piruvato, también de 3 carbonos. Dos moléculas de NAD+ se reducen cuando las triosas se oxidan.
Además, la hexosa inicial es fosforilada dos veces a expensas del ATP. Después de la escisión, cada molécula de tres carbonos es fosforilada una vez más, en este caso, a partir de fosfato inorgánico. Las uniones de todos los fosfatos incorporados son llevadas a uniones de alta energía y los fosfatos son transferidos al ATP. Las dos fosforilaciones a nivel de sustrato rinden 4 ATP. Descontando los dos ATP invertidos en los pasos 1 y 3, la glucólisis produce una ganancia neta de 2 ATP.
Balance de la glucólisis |
Sustratos |
Productos |
| glucosa |
2 piruvato |
| 2 NAD+ |
2 NADH |
| 2 ATP + 2 P |
2 ATP |
Descarboxilación oxidativa del piruvato Regresar
Balance de descarboxilación del piruvato |
Sustratos |
Productos |
| Piruvato + CoA + NAD+ |
Acetil-CoA + CO2 + NADH |
El piruvato obtenido como producto de la glucólisis ingresa a la matriz mitocondrial, donde continúa la respiración aeróbica.
La descarboxilación oxidativa es una reacción que consiste en la pérdida del grupo carboxilo y la deshidrogenación del piruvato.
El grupo carboxilo separado del piruvato se elimina como dióxido de carbono (CO2). Esta reacción es una de las fuentes del dióxido de carbono que difunde hacia la sangre y se libera a través del pulmón.
El hidrógeno liberado por cada piruvato se transfiere a la coenzima NAD+.
Como producto de las transformaciones sufridas por el piruvato se obtiene una molécula de dos carbonos, el grupo acetilo, que es captado por la Coenzima A, formando el complejo acetil-CoA.
Ciclo de Krebs Regresar
El ciclo de Krebs es la etapa final de la degradación del combustible. Se trata de un conjunto de reacciones que transcurren en la matriz mitocondrial. Al cabo de las mismas, lo que queda del combustible (el grupo acetilo) se descompone y deshidrogena, de manera que se liberan dos moléculas de CO2 (el cual difunde hacia el exterior), mientras que sus átomos de hidrógeno son captados por el NAD+ y el FAD. También ocurre una fosforilación a nivel de sustrato, que da como resultado una molécula de GTP.
El ciclo de Krebs recibe este nombre, pues uno de sus sustratos, el oxalacetato, se regenera en la reacción final.
Las reacciones del ciclo de Krebs pueden agruparse en tres etapas:
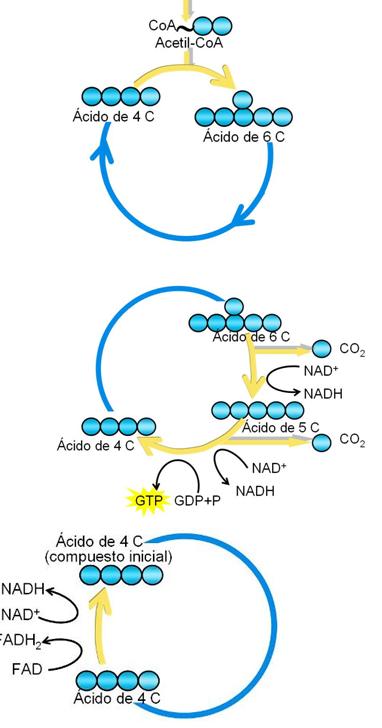 |
1ª Etapa. El ciclo de Krebs comienza cuando el grupo acetilo, de 2 C, es transferido desde la CoA a un compuesto iniciall de 4 C, presente en la mitocondria (oxalacetato). La condensación de ambos da lugar a la formación de un compuesto de 6 C, el citrato o ácido cítrico. |
2ª Etapa. El ácido de 6 C sufre una descarboxilación oxidativa. Se obtienen CO2, NADH y un ácido de 5 C, el cetoglutarato. Una nueva descarboxilación oxidativa ocurre al ácido de 5 C, produciendo como resultado un ácido de 4 C. A esta reacción se acopla una fosforilación a nivel de sustrato, generando GTP.
|
3ª Etapa. El intermediario de 4 C es deshidrogenado dos veces, reduciendo, sucesivamente, al FAD y al NAD+. Finalmente, se regenera el compuesto inicial. |
El Ciclo de Krebs paso a paso Regresar
Balance del Ciclo de Krebs Regresar
Balance del Ciclo de Krebs |
Sustratos |
Productos |
| Acetil-CoA |
2 CO2 + CoA |
| 3 NAD+ |
3 NADH |
| FAD |
FADH2 |
| GDP + Pi |
GTP |
Partiendo de una molécula de glucosa, se obtienen 2 moléculas de piruvato. Cada una de ellas aporta un grupo acetilo, que ingresa al ciclo de Krebs transportado por la Coenzima A. Por lo tanto, el balance del ciclo de Krebs debe multiplicarse por 2 al realizar la cuenta final.
Cadena respiratoria Regresar
A lo largo de las fases precedentes –glucólisis, descarboxilación del piruvato y ciclo de Krebs- se donan electrones de alta energía y protones desde los compuestos intermediarios de estas vías metabólicas a las coenzimas NAD+ y FAD. Las formas reducidas de las mismas, NADH y FADH2, son ricas en energía; en ellas se conserva la mayor parte de la energía proveniente del combustible. A continuación, el NADH y el FADH2 ceden sus electrones a la cadena respiratoria.
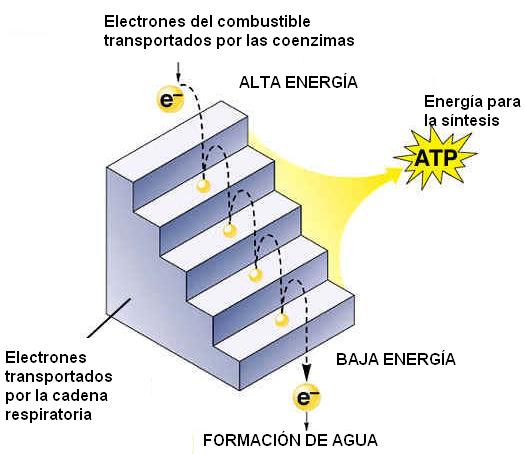 |
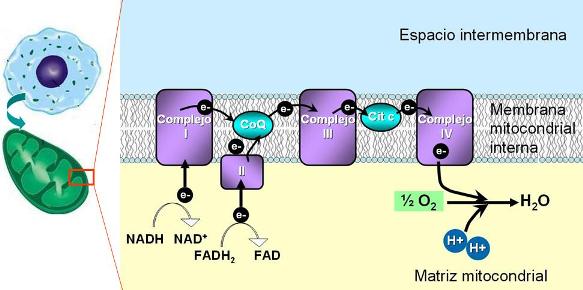
La cadena respiratoria es una cadena transportadora de electrones. Está formada por cuatro complejos proteicos, (I, II, III y IV), tres de ellos transmembranares, presentes en la membrana mitocondrial interna. Los complejos están ligados por dos compuestos solubles, que tienen movilidad lateral dentro de la membrana: la ubiquinona (coenzima Q) y el citocromo c.
Los transportadores de electrones que conforman la cadena se disponen en la membrana por orden de afinidad electrónica creciente.
La cadena de transporte de electrones es iniciada por el NADH, que cede un par de electrones al complejo I, y el FADH2, que cede sus electrones al complejo II.
Cada complejo se reduce al recibir un par de electrones y luego se oxida, cuando los cede al siguiente transportador de la cadena.
Durante el pasaje por la cadena de transporte, los electrones de alta energía van perdiendo gran parte de su energía; la energía liberada es utilizada para promover la síntesis de ATP.
El último transportador de la cadena respiratoria cede los electrones al oxígeno molecular (O2). Éste se reduce y capta protones, formando agua.
 |
Balance de la cadena respiratoria |
Sustratos |
Productos |
| NADH |
NAD+ |
| FADH2 |
FAD |
| O2 |
H2O |
El oxígeno molecular debe estar presente en la mitocondria para que la cadena de transporte de electrones no deje de funcionar. Cuando falta el oxígeno, los transportadores no pueden reoxidarse, pues no hay aceptor final para los electrones. De la misma forma, el NADH y el FADH2 permanecen reducidos. Al agotarse las reservas de NAD+ y FAD, tampoco es posible la continuidad de las vías que los requieren como sustratos.
Por lo tanto, si bien el O2 tan sólo es sustrato de la cadena respiratoria, su presencia es imprescindible para que se lleven a cabo las etapas anteriores de la respiración aeróbica.
Además, la disponibilidad de O2 es fundamental por cuanto la síntesis de ATP por fosforilación oxidativa, el mecanismo que rinde la mayor parte del ATP obtenido de la respiración, depende directamente del funcionamiento de la cadena respiratoria, como veremos a continuación.
Fosforilación oxidativa e Hipótesis quimiosmótica Regresar
El transporte de electrones por la cadena respiratoria está acoplado al transporte de protones a través de la membrana mitocondrial interna, desde la matriz mitocondrial hasta el espacio intermembrana. Mientras los electrones fluyen por la cadena de óxido-reducción, los protones son transferidos desde un compartimiento mitocondrial al otro, en tres lugares específicos.
Los sitios de bombeo de protones son los complejos I, III y IV de la cadena transportadora. Los electrones provenientes del NADH promueven el bombeo de protones en los tres complejos. Los electrones que provienen del FADH2, en cambio, sólo lo hacen a través de los complejos III y IV, ya que son entregados directamente al complejo II, sin pasar por el complejo I.
A medida que ocurre el bombeo de protones a través de los complejos, se va generando un gradiente electroquímico. Los protones tienen tendencia a regresar hacia la matriz, siguiendo su gradiente.
Sin embargo, el gradiente se mantiene, puesto que la membrana mitocondrial interna es impermeable a los protones. De esta forma, los protones concentrados en el espacio intermembrana acumulan energía potencial.
En la membrana mitocondrial interna se ubican las partículas submitocondriales o partículas respiratorias. Se trata de complejos proteicos que constan de dos partes: la porción Fo, un tallo inserto en el espesor de la membrana, y la porción F1, que se proyecta hacia la matriz mitocondrial.
El tallo Fo posee un canal en su interior, la única vía por donde los protones pueden regresar hacia la matriz, a favor de su gradiente.
La porción F1 es una enzima con actividad ATP sintetasa. Cuando los protones atraviesan el tallo Fo de regreso, la energía liberada activa a la ATP sintetasa. Ésta cataliza la síntesis de ATP, a partir de ADP y fosfato.
La síntesis de ATP acoplada a la cadena respiratoria recibe el nombre de fosforilación oxidativa.
En conclusión:
- El transporte de electrones por la cadena respiratoria se asocia con un bombeo de protones.
- El bombeo de protones genera un gradiente electroquímico, una forma de energía potencial.
- Los complejos Fo-F1 utilizan la energía liberada en el pasaje de protones para la síntesis de ATP. |
Balance de la Fosforilación oxidativa |
Sustratos |
Productos |
| ADP + P + Energía |
ATP |
Si bien aún se desconocen muchos detalles de la forma en que la cadena respiratoria se acopla con la fosforilación oxidativa, esta explicación, conocida como hipótesis quimiosmótica (que fue propuesta por Mitchell en 1981) es la más aceptada en la actualidad.
Cantidad de ATP sintetizado en la fosforilación oxidativa
Por cada NADH que activa la cadena respiratoria -> 3 ATP
Por cada FADH2 que activa la cadena respiratoria -> 2 ATP |
Teniendo en cuenta la cantidad de protones bombeados por cada complejo durante el transporte de electrones, se calcula que los electrones entregados por cada NADH a la cadena respiratoria contribuyen a la síntesis de 3 ATP, en tanto que los cedidos por cada FADH2 proporcionan energía para la síntesis de 2 ATP.
La fosforilación oxidativa es la principal fuente de ATP en la célula.
Balance energético de la respiración aeróbica Regresar
El balance del ATP sintetizado durante la respiración aeróbica a partir de una molécula de glucosa es el siguiente:
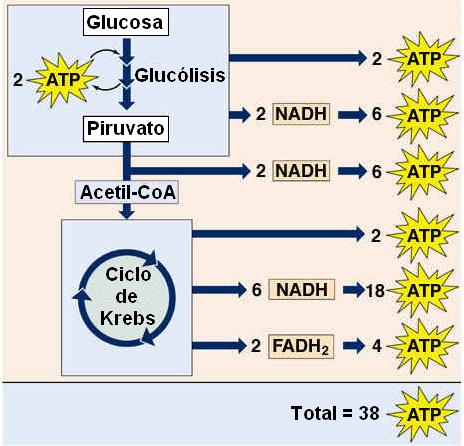 |
El número máximo teórico de ATP que es posible obtener al final de la respiración aeróbica es igual a 38.
Se obtienen 2 ATP por fosforilación a nivel de sustrato durante la glucólisis y 2 GTP por el mismo mecanismo durante el ciclo de Krebs. El GTP es fácilmente convertido en ATP, transfiriendo el grupo fosfato desde este último al GDP.
Además, se contabilizan las moléculas de ATP sintetizadas por fosforilación oxidativa acoplada a la cadena respiratoria: 3 ATP por cada NADH y 2 ATP por cada FADH2 que ingresan a la cadena de transporte de electrones.
Sin embargo, en algunos casos, este balance puede verse reducido a 36 ATP. Esta merma obedece a que las coenzimas NADH producto de la glucólisis se generan en el citosol, a diferencia de las demás coenzimas reducidas durante la descarboxilación del piruvato y el ciclo de Krebs, que se encuentran en la matriz mitocondrial. Los electrones del NADH proveniente de la glucólisis deben llegar a la matriz mitocondrial, a fin de que puedan ser entregados a la cadena respiratoria. El pasaje de los electrones a través de ambas membranas mitocondriales se realiza mediante un mecanismo denominado “lanzadera”, en el que los electrones son transferidos a compuestos intermediarios y finalmente a una coenzima ubicada en la matriz de la mitocondria. Existen distintas lanzaderas, según el tipo celular. En un tipo de lanzadera, el aceptor de los electrones en la mitocondria es el NAD+; en otro tipo, el FAD. En el segundo caso, la cantidad de ATP obtenida por fosforilación oxidativa a partir de la glucólisis es de 4 en lugar de 6 ATP, lo que cambia el total de 38 a 36 ATP.
 |
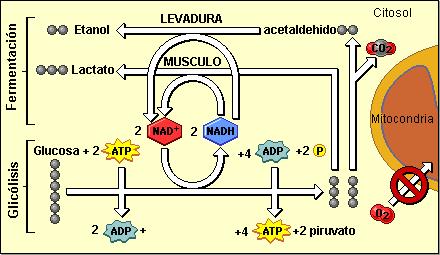
Fermentación Regresar
Los procesos anaeróbicos son típicos de ciertas bacterias (células procariotas) y de las levaduras (hongos unicelulares eucariotas).
Las células eucariotas son aeróbicas, salvo algunas excepciones. Ya se mencionó el caso de los glóbulos rojos, células que carecen de mitocondrias en su estadío maduro y el de las células musculares, que son anaeróbicas facultativas, esto es: llevan a cabo una oxidación anaeróbica cuando el abasto de oxígeno no es suficiente.
La oxidación anaeróbica transcurre enteramente en el citosol y consta de dos etapas: glucólisis y fermentación. De ellas, sólo la glucólisis aporta ATP.
La fermentación consiste en la reducción del piruvato, que acepta los protones y electrones transportados por el NADH generado en la glucólisis.
El producto final que se obtiene de la reducción del piruvato depende del tipo celular. En levaduras ocurre la fermentación “alcohólica”: el piruvato es descarboxilado, rindiendo dióxido de carbono y acetaldehído, y luego éste es reducido a etanol.
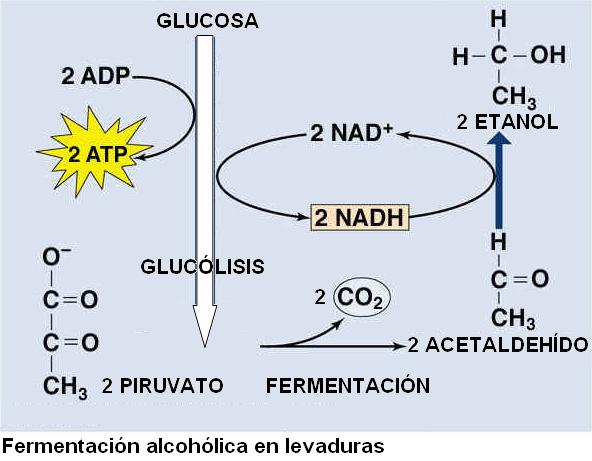 |
En las células animales, el piruvato es reducido a lactato o ácido láctico. Este tipo de fermentación se denomina “láctica”.
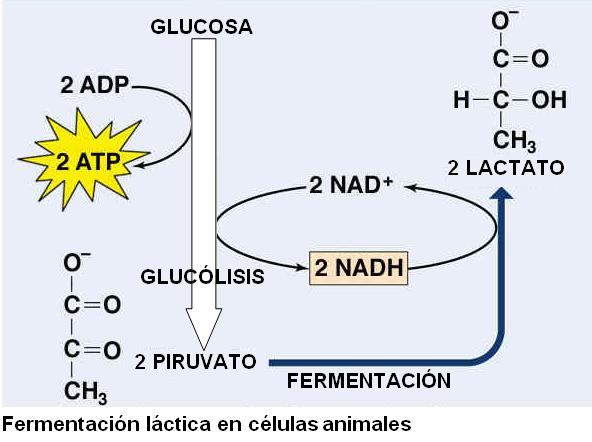 |
¿Cuál es el “objetivo” de la fermentación? Es importante recordar que la fosforilación a nivel de sustrato tiene lugar en los pasos 6 y 9 de la glucólisis, durante los cuales se recupera el ATP invertido en los primeros pasos y se obtiene la ganancia neta de 2 ATP. Previamente, en el paso 5, se requiere la presencia de NAD+ como sustrato; en esta reacción se produce la reducción del NAD+ a NADH. Cuando no funciona la vía aeróbica, el NADH no puede ser reoxidado en la cadena respiratoria. Entonces la coenzima oxidada (NAD+) se convierte en un factor limitante de la glucólisis. La falta de NAD+ interrumpe la vía glucolítica antes de la generación de ATP, a menos que el NADH pueda ser reoxidado en otra reacción, independiente de oxígeno.
La función de la fermentación es, precisamente, la de proveer NAD+ en condiciones anaeróbicas, permitiendo así la continuidad de la glucólisis y la ganancia neta de 2 ATP, como balance energético total de la respiración anaeróbica.
 |
Cuando se realizan ejercicios muy intensos, el organismo no llega a proveer a las células musculares del oxígeno suficiente para la respiración aeróbica. Ante esta imposibilidad, el tejido muscular obtiene energía de la glucólisis, con la consecuente producción de lactato. La acumulación de lactato en el tejido muscular produce calambres musculares. También puede ocasionar una acidosis láctica leve, en la que el pH sanguíneo está por debajo de los valores normales.
Situaciones más extremas, como infarto de miocardio o hemorragias severas, producen un colapso circulatorio e hipoxia tisular. En esos casos hay acidosis láctica grave.
El lactato presente en la circulación es captado por el hígado, donde se utiliza para la síntesis de glucosa (ciclo de Cori).
Resumen Regresar
| CONDICIÓN |
AERÓBICA |
ANAERÓBICA |
| ETAPAS |
- Glucólisis
- Descarboxilación oxidativa
- Ciclo de Krebs
- Cadena respiratoria
- Fosforilación oxidativa
|
|
| RENDIMIENTO ENERGÉTICO |
36 - 38 ATP |
2 ATP |
| ECUACIÓN GLOBAL |
Glucosa + 6 O2 -> 6 CO2 + 6 H2O |
Glucosa -> 2 Lactato |
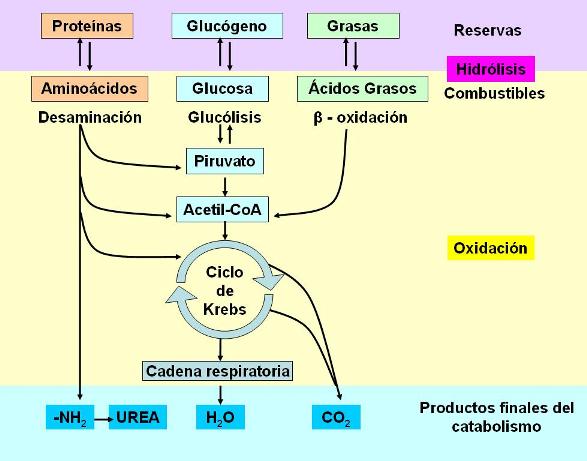
Oxidación de Ácidos grasos y Aminoácidos Regresar
Los ácidos grasos y los aminoácidos también son utilizados como combustibles.
Los ácidos grasos se obtienen de la dieta, o bien de la hidrólisis de los depósitos de grasa del tejido adiposo. Antes de ingresar a la respiración celular, los ácidos grasos son transformados en acetil-CoA, dentro de la mitocondria, en un proceso denominado beta oxidación. Cada molécula de acetil-CoA obtenida se incorpora al ciclo de Krebs.
Los aminoácidos se utilizan como combustibles en dos situaciones: cuando su disponibilidad en el organismo supera la capacidad de utilización de los mismos en la síntesis de proteínas, o bien cuando no existe otra fuente de energía. En el último caso, las proteínas corporales son hidrolizadas para proporcionar los aminoácidos que las constituyen.
Los aminoácidos pueden oxidarse previa desaminación. La desaminación tiene lugar en el hígado y consiste en la liberación del grupo amino, posteriormente convertido en urea y eliminado por la orina. El resto del aminoácido, un cetoácido, ingresa a la respiración celular en la glucólisis, como piruvato, como acetil-CoA, o algún otro intermediario del ciclo de Krebs, dependiendo del aminoácido del cual derive.
El ciclo de Krebs constituye, por lo tanto, la vía final común en el catabolismo de los compuestos orgánicos.
 |
|
|
